
【題目】自然界中無時不在進行著氧氣、二氧化碳、水的循環,使地球充滿勃勃生機.
(1)地球大氣中二氧化碳含量增多,會產生_____,導致全球變暖。
(2)對維持大氣中二氧化碳氣體含量相對穩定,最重要的反應是______
ACO2+H2O=H2CO3 BCO2+NaOH=Na2CO3+H2O
CCO2+ C ![]() 2CO D6CO2 +6H2O
2CO D6CO2 +6H2O![]() 6C6H12O6+6O2
6C6H12O6+6O2
(3)飲用硬度過大的水都不利于人體健康.可通過_____方法來降低水的硬度。
(4)相同條件下氣體體積之比等于分子數之比,則空氣中氧分子與氮分子總質量之比為__________。
科目:初中化學 來源: 題型:
【題目】如圖1是以石灰石為原料制備高純超細碳酸鈣的工藝流程圖:

(1)流程中操作A的名稱_____。實驗室里該操作用到的玻璃儀器有燒杯、_____和_____。
(2)主要反應原理:
①“煅燒”步驟:主要反應的化學方程式為_____,反應基本類型為_____反應。
②“浸出”步驟:CaO+2NH4Cl=CaCl2+H2O+2NH3↑。
③“碳化”步驟:CO2+2NH3+H2O+CaCl2=CaCO3↓+2 NH4Cl。
(3)煅燒石灰石得到的固體中,除含CaO外,還含有少量MgO、FeO等雜質,在“浸出”過程為保證鐵、鎂等雜質不被浸出,需要適當提高溶液的pH.根據反應②計算出的鈣銨比(參加反應的氧化鈣和氯化銨的質量比)為_____,而實際流程中最佳鈣銨比要稍高于這一比值,原因是_____。
(4)用上述流程可循環使用的物質除了H2O、CO2和NH3之外,還有_____。
(5)實驗室在如圖2裝置中模擬上述流程制備高純超細碳酸鈣:

①攪拌的作用是_____。
②制備CaCl2溶液時需要對裝置加熱,主要作用是_____。
A 加快反應速率 B 促進氨氣逸出
③已知在常溫和一個標準大氣壓下,CO2和NH3在100g水中分別能溶解0.169g和52.9g。制備CaCO3時應先通入氨氣后通入二氧化碳,理由是_____。
④浸取一步中NH4Cl溶液的溶質質量分數直接影響著生成CaCl2溶液溶質質量分數。已知0﹣100℃時NH4Cl的溶解度如下表:
溫度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解(g) | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
如果用200g 80℃時NH4Cl的飽和溶液與純氧化鈣恰好完全反應,計算充分反應后得到CaCl2的質量_____。(寫出計算過程,保留一位小數。)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】我國高純氧化鎂產品供不應求,工業上可以用硫酸鎂還原熱解制備,工業流程如下:

(1)菱鎂礦主要成分是碳酸鎂,反應前要粉粹,目的是______,反應1化學反應方程式為___________。
(2)反應2中的化學方程式為:2MgSO4+C![]() 2MgO+2SO2↑+______。
2MgO+2SO2↑+______。
(3)反應2中硫酸鎂與炭的配比對硫酸鎂轉化率的影響如下圖1,硫酸鎂轉化率最高時m(MgSO4):m(C)=______,當配炭比2:1~3:1時硫酸鎂轉化率低的原因是______。
(4)反應2中時間和溫度對硫酸鎂轉化率的影響分別如下圖2、圖3,則最佳的時間和溫度分別為______h、______℃。

(5)尾氣直接排放到空氣中會引起______、______兩個當今世界全球性問題,可以用石灰漿吸收其中的有毒氣體,化學方程式為:______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在一密閉容器中加入甲、乙、丙、丁四種物質,在下定條件下發生化學反應,測得反應前及t1、t2時各物質質量如右圖所示。下列說法中不正確的是

A.該反應為化合反應
B.該反應中,乙、丁的質量變化之比為7:5
C.丙可能為該反應的催化劑
D.該反應中,甲、乙的質量變化之比為1:4
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】溶解度可表示物質溶解性的大小
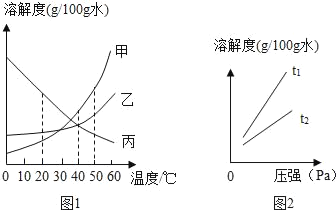
①如圖1是甲、乙、丙三種固體物質(均不含結晶水)的溶解度曲線
Ⅰ.20℃時,甲的溶解度_____(填“>”、“<”或“=”)乙的溶解度。
Ⅱ.40℃時,乙和丙_____(填“能”或“不能”)形成溶質質量分數相同的飽和溶液。
Ⅲ.20℃時,燒杯中分別盛有相同質量甲、乙、丙的飽和溶液,各加入等質量的對應固體,并升溫至50℃.請填寫下表。
燒杯中的溶質 | 燒杯中固體的變化 |
甲 | _____ |
乙 | 固體逐漸減少至全部溶解 |
丙 | _____ |
Ⅳ.若分別將100g乙、丙的飽和溶液從50℃降溫到40℃,對所得溶液的敘述正確的_____(填序號)。
A 乙、丙都是飽和溶液 B 所含溶劑質量:乙<丙
C 溶液質量:乙>丙 D 溶質質量分數:乙>丙
②氣體的溶解度也有一定的變化規律。
Ⅰ.打開可樂瓶,逸出大量氣泡.由此可見,壓強越小,CO2的溶解度越_____.為增大CO2的溶解度,可采用的一種方法是_____。
Ⅱ.不同溫度下,氧氣的溶解度隨壓強的變化如圖2所示,圖中t1對應的溫度為40℃,則t2對應的溫度_____(填編號)。
a 小于40℃ b 大于40℃ c 無法確定
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖為KNO3、NaNO2(亞硝酸鈉)、NaCl的溶解度曲線,下列說法正確的是
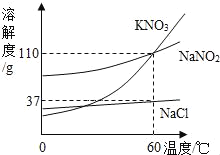
A. KNO3和NaNO2的溶解度相等
B. 60 ℃時,NaCl的飽和溶液的溶質質量分數為37%
C. 將接近飽和的NaNO2溶液變為飽和溶液,可采用降溫的方法
D. 除去NaCl中少量KNO3,可在較高溫度下制得濃溶液再冷卻結晶、過濾、干燥
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某科研小組設計利用稀H2SO4浸取某廢棄的氧化銅鋅礦(主要成分為CuO和ZnO,其余成分既不與酸反應,也不溶解于水)的方案,實現廢物綜合利用。部分實驗流程如下:
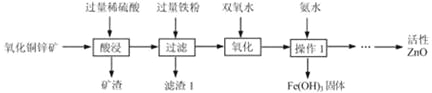
請根據上述實驗流程回答下列問題:
(1)操作1的名稱是 。
(2)在氧化銅鋅礦中加入過量稀硫酸,主要成分發生反應的化學方程式為 , 。
(3)加過量鐵粉后,發生反應的基本反應類型是 ,得到濾渣1的成分為 (填化學式)。
(4)在實驗過程中,雙氧水會與Fe2+反應生成Fe3+和水,以便在后續的操作中將溶液中鐵元素除去。高錳酸鉀溶液也能將Fe2+氧化成Fe3+,選用雙氧水的優點是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(題文)國際上有銦等7種元素的相對原子質量采用了我國科學家張青蓮測的數據。由如圖可知銦元素
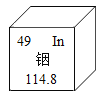
A. 是非金屬元素
B. 質子數為49
C. 相對原子質量是114.8克
D. 與其他元素根本區別是中子數不同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com