
【題目】(5分)雞蛋殼的主要成分是碳酸鈣.小明同學為了測定雞蛋殼中碳酸鈣的質量分數,分別設計了如下實驗并進行計算.將雞蛋殼洗凈、干燥并搗碎后放入錐形瓶里,加入足量的稀鹽酸充分反應(假設其他雜質不與鹽酸反應).
測得相關數據如圖所示:

【數據處理】
(1)反應生成二氧化碳的質量為 g.
(2)請幫小明計算雞蛋殼中碳酸鈣的質量分數,并寫出計算過程:
實驗過程如果有部分生成的二氧化碳氣體因溶解于水而沒有全部逸出,造成計算結果與實際值相比 (填“偏大”、“偏小”或“不變”)
【答案】(5分)(1)4.4g(1分)(2)解:設雞蛋殼中碳酸鈣的質量為x.
CaCO3+2HCl=CaCl2+H2O+CO2↑ …………………1分
100 44
x 4.4g
![]() =
=![]()
x=![]()
![]() =10g………………………………………1分
=10g………………………………………1分
雞蛋殼中碳酸鈣的質量分數為:![]() ×100%=80% ………1分
×100%=80% ………1分
答:雞蛋殼中碳酸鈣的質量分數為80%。 偏小(1分)
【解析】
試題分析:(1)由質量守恒定律可知生成 二氧化碳質量為12.5+40.5-48.6=4.4克。
(2)解:設雞蛋殼中碳酸鈣的質量為x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
![]() =
=![]()
x=![]()
![]() =10g
=10g
雞蛋殼中碳酸鈣的質量分數為:![]() ×100%=80% ………1分
×100%=80% ………1分
答:中碳酸鈣的質量分數為80%。
實驗過程中如果有部分生成的二氧化碳氣體因溶解于水而沒有全部逸出,造成計算結果與實際值相比偏小。


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
【題目】全國有40個重點城市開展“綠箱子環保計劃——廢棄手機及配件回收聯合行動”,下列有關廢棄手機中的金屬材料回收利用的說法不正確的是
A.可以節約金屬資源
B.可以節約冶煉相關金屬所消耗的能源
C.可以減少對環境的污染
D.回收廢棄手機中的金屬材料沒有任何價值
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某農田出現了土壤酸化板結的現象,經調查,該農田長期施用化肥(NH4)2SO4.下列推測中,錯誤的是( )
A.(NH4)2SO4溶液的pH可能小于7
B.土壤板結可能是長期施用(NH4)2SO4造成的
C.為了防止土壤酸化,施用(NH4)2SO4的同時應加入Ca(OH)2
D.草木灰(主要含K2CO3)可改良酸性土壤,說明K2CO3的溶液可能呈堿性
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(5分)請結合下列實驗常用裝置,回答有關問題.
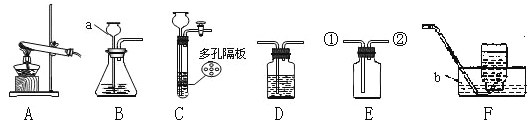
(1)儀器a的名稱是 。
(2)若用B、F組成制取某氣體的裝置,寫出制取此氣體的化學方程式為 ,
若要獲得干燥的二氧化碳,除發生裝置外,還應選用D裝置,并在該裝置中盛放 試劑(填寫試劑名稱).如果用E裝置收集該氣體則氣體從 端進入(填“①”或“②”)。
(3)乙炔(C2H2)是無色、無味、易燃的氣體,乙炔的密度比空氣略小,難溶于水。乙炔(C2H2)氣體和氧氣反應能產生高溫火焰,工人師傅常用氧炔焰切割或焊接金屬。乙炔由碳化鈣(塊狀固體)與水反應生成,同時生成一種白色固體。已知碳化鈣與水反應非常劇烈。實驗室欲制取并收集純凈的乙炔,要求做到節約、安全、隨時發生、隨時停止,你選擇的裝置是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(4分)A圖為實驗示意圖,在室溫情況下,燒杯中盛裝的是甲物質的溶液,試管①中盛裝的是乙物質的溶液,試管②中盛裝的是丙物質的溶液。當它們由室溫升到80℃時,發現燒杯中甲物質沒有明顯變化,而試管①中盛裝的是乙物質全部溶解,試管②中有丙物質析出。B圖表示三種物質的溶解度曲線。請你據此現象回答下列有關問題:
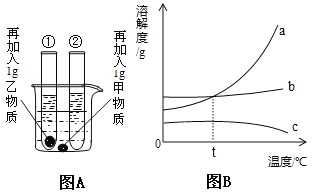
(1)室溫時, (選填“燒杯”、“試管①”或“試管②”)中溶液可能是不飽和溶液;
(2)上圖能表示甲物質的溶解度曲線的是 (選填a、b或c);
(3)若乙物質溶液中混有少量的甲物質,提純乙物質可采取的方法是
(4)對于甲、乙兩物質飽和溶液,在溫度 時,乙物質的溶質質量分數一定比甲物大.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知空氣的主要成分是氮氣和氧氣。某課外活動小組設計了測定空氣中氧氣含量的實驗,實驗裝置如下圖所示。(6分)
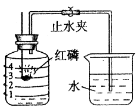
(1)紅磷在集氣瓶中發生反應的文字表達式為:
該實驗中紅磷需稍過量,目的是 。
(2)待燃燒停止,白煙消失并冷卻后,打開止水夾,觀察到燒杯中的水進入集氣瓶,瓶內水面最終接近刻度1處。由此可知,氧氣約占空氣總體積的 ,由本實驗還可推知氮氣的哪一些性質?試寫出其中的一種:
(3)若將紅磷換成碳粉,該實驗能否獲得成功? (填“能”或“否”)
(4)人類需要潔凈的空氣,目前我國城市空氣質量日報中的污染物主要包括
A、一氧化碳
B、二氧化碳
C、二氧化硫
D、可吸入顆粒物
E、二氧化氮
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】亞硝酸鈉是實驗室常用的試劑,實驗室一般用亞硝酸鈉溶液與氯化銨溶液反應來制取N2。N2的化學性質十分穩定,但在一定條件下能與H2部分化合生成NH3。下圖為制取少量NH3的裝置(制取H2的裝置已略去):
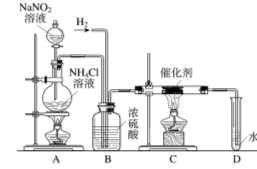
(1)寫出上圖中你最熟悉的兩種儀器名稱:
①_________________,
②__________________。
(2)寫出C裝置的硬質試管中發生反應的化學方程式____________________。
(3)反應時N2和H2的最佳質量比是________。如果按此比例進行反應,反應時,D中導管口是否會逸出氣泡?(已知NH3極易溶于水),說明逸出氣泡的原因:______________________
(4)B中濃硫酸的作用是___________________。
(5)用實驗方法證明確實有NH3生成:_____________________________。
(6)歸納與演繹是重要的科學方法,也是常用的學習方法。我們已經學過實驗室制取氣體的反應原理、制取與收集方法。請你歸納出實驗室制取氣體反應的共同點:
________________(填序號)。
①需要加熱
②使用催化劑
③沒有氣體參加反應
④原料為純凈物
⑤只生成一種氣體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com