
【題目】氯化鈉是重要的化工原料,氯堿工業生產的一種流程如圖:

(1)從“海水葉粗鹽葉精鹽”的過程包括溶解、過濾、蒸發等實驗操作,實驗室中上述3種操作都需要使用的儀器是_____(填名稱),該儀器在蒸發操作中的作用是_____。
(2)“食鹽水”中常含有NaCl,MgCl2,CaCl2等物質,“精制”過程中加入NaOH的目的是_____。
(3)20℃時,“飽和食鹽水”的溶質質量分數為26.47%,則該溫度下,氯化鈉的溶解度為_____(計算結果精確到0.1)。
(4)寫出“電解槽”中發生反應的化學方程式:_____。
(5)流程中可以循環使用的物質有_____(填化學式)。
(6)氯堿工業生產的堿樣品中常含有Na2CO3和NaCl等雜質,堿樣品中含有Na2CO3的原因是_____;檢驗堿樣品中是否含有Na2CO3,下列試劑中可選擇使用的是_____(填字母)。
A 酚酞試液 B 石蕊試液 C 硝酸銨溶液 D 澄清石灰水
(7)用“離子交換膜法”生產的堿樣品質量主要標準如下表所示:
等級 | 氫氧化鈉含量 | 碳酸鈉含量 |
優等品 | ≥99.0% | ≤0.5% |
一等品 | ≥98.5% | ≤0.8% |
合格品 | ≥98.0% | ≤1.0% |
化學興趣B組設計并完成了如下實驗來判斷堿樣品的等級(不考慮其他雜質參加反應)。稱取20.3 g堿樣品,加入足量的水溶解,再加入足量的氯化鋇溶液,充分反應后,過濾得到濾渣和濾液;將濾渣洗滌、干燥,得到碳酸鋇固體0.197 g;向濾液中加入2滴酚酞,再逐滴加入稀鹽酸至恰好完全反應,共消耗溶質質量分數為5.0%的稀鹽酸365 g。
①該堿樣品中碳酸鈉的含量(質量分數)為_____(計算結果精確到0.01% )。
②列式計算該堿樣品中氫氧化鈉的含量_____(計算結果精確到0.01% )。
③該堿樣品的等級為_____。
【答案】玻璃棒 攪拌,防止受熱不均而發生迸濺 除去氯化鎂 36.0g 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ NaCl和NaOH 氫氧化鈉接觸空氣變質生成碳酸鈉 D 0.52% 98.52% 一等品
2NaOH+H2↑+Cl2↑ NaCl和NaOH 氫氧化鈉接觸空氣變質生成碳酸鈉 D 0.52% 98.52% 一等品
【解析】
(1)從“海水葉粗鹽葉精鹽”的過程包括溶解、過濾、蒸發等實驗操作,實驗室中上述3種操作都需要使用的儀器是 玻璃棒,該儀器在蒸發操作中的作用是 攪拌,防止受熱不均而發生迸濺。
(2)“食鹽水”中常含有NaCl,MgCl2,CaCl2等物質,由于氫氧化鎂是難溶性物質,所以“精制”過程中加入NaOH的目的是 除去氯化鎂。
(3)20℃時,“飽和食鹽水”的溶質質量分數為26.47%,設該溫度下氯化鈉的溶解度為S,則有![]() ×100%=26.47%,則S≈36.0g。
×100%=26.47%,則S≈36.0g。
(4)“電解槽”中發生反應是氯化鈉溶液在通電的條件下生成氫氧化鈉和氫氣以及氯氣,對應的化學方程式為:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(5)流程中可以循環使用的物質有 NaCl和NaOH(填化學式)。
(6)氯堿工業生產的堿樣品中常含有Na2CO3和NaCl等雜質,堿樣品中含有Na2CO3的原因是 氫氧化鈉接觸空氣變質生成碳酸鈉;檢驗堿樣品中是否含有Na2CO3,由于是檢驗氫氧化鈉中是否有碳酸鈉,而兩者均顯堿性,所以不能借助酸堿性進行區別,而是借助氫氧根和碳酸根的區別,所以應該選用澄清石灰水。故選D。
(7)稱取20.3 g堿樣品,加入足量的水溶解,再加入足量的氯化鋇溶液,充分反應后,過濾得到濾渣和濾液;將濾渣洗滌、干燥,得到碳酸鋇固體0.197 g;向濾液中加入2滴酚酞,再逐滴加入稀鹽酸至恰好完全反應,共消耗溶質質量分數為5.0%的稀鹽酸365 g。
①設該堿樣品中碳酸鈉的質量分數為x,該堿樣品中氫氧化鈉的質量分數為y
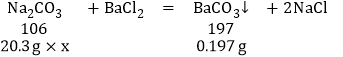
![]() =
=![]()
x≈0.52%

![]() =
=![]()
y≈98.52%
符合一等品標準,為一等品
故答案為:
(1)玻璃棒; 攪拌,防止受熱不均而發生迸濺。
(2)除去氯化鎂。
(3)36.0g。
(4)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(5)NaCl和NaOH。
(6)氫氧化鈉接觸空氣變質生成碳酸鈉; D。
(7)①0.52%
②98.52%
③一等品。


科目:初中化學 來源: 題型:
【題目】信息時代,5G讓手機飛起來!手機芯片是智能手機終端的關鍵。制備該電子芯片的主要材料是硅,可以利用石英砂(主要成分是SiO2)制得,試回答下列問題。

①工業上制取硅的主要反應為:SO2+2C![]() Si+2CO,該反應的反應物中屬于氧化物的是_____,生成的一氧化碳中碳元素的化合價為_____,該反應屬于_____反應(填“分解”“化合”“置換”“復分解”之一)。
Si+2CO,該反應的反應物中屬于氧化物的是_____,生成的一氧化碳中碳元素的化合價為_____,該反應屬于_____反應(填“分解”“化合”“置換”“復分解”之一)。
②二氧化硅還是生產玻璃的主要原料之一。下列有關材料的說法中,不正確的是_____(填寫序號)。
A 玻璃是無機非金屬材料
B 玻璃鋼屬于金屬材料
C 塑料是有機高分子材料
D 生鐵和鋼都屬于合金
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室常用過氧化氫溶液和二氧化錳(催化劑)制取氧氣。
【提出問題】催化劑二氧化錳的用量對反應速率是否有影響?
【設計實驗】(1)實驗裝置如圖所示:
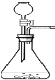

![]() (2)實驗記錄:實驗數據如下表:
(2)實驗記錄:實驗數據如下表:
過氧化氫體積(ml) | 過氧化氫濃度 | 二氧化錳質量(g) | 測量數據(ml) | |
Ⅰ | 30 | 5% | 0.1 | |
Ⅱ | 30 | 5% | 0.2 | |
Ⅲ | 30 | 5% | 0.3 |
【實驗分析】(1)過氧化氫分解的文字表達式為____________________;二氧化錳可作為該反應的催化劑的依據是__________________。
(2)表格中的“測量數據”是:相同時間內_______________________
(3)本實驗中,測定待測數據的裝置(上圖中虛線框里)是_______(填編號)。

(4)若第Ⅱ次比第Ⅲ次實驗的“測量數據”更______(填“大”或“小”)說明催化劑的用量越多,反應更快。
【實驗反思】除了上述因素會影響過氧化氫的反應速率外,_________(寫一種)也會影響過氧化氫的分解反應速率,請寫出你的實驗方案:_______________________
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某興趣小組在實驗室發現一瓶敞口久置的氫氧化鈉,為測定氫氧化鈉的變質情況,他們取9.3g變質的氫氧化鈉樣品于錐形瓶中,加入50g水,充分溶解,逐漸加入未知濃度的H2SO4溶液,生成的氣體與加入硫酸的質量如圖所示:
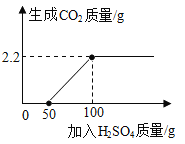
(1)加入稀H2SO4的質量在0~50g時;稀H2SO4與_____發生反應,其反應實質是_____。
(2)所用樣品中氫氧化鈉的質量分數是多少_____?(精確到0.1%)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】昆山化學教研員提醒您﹣“實驗千萬個,安全第一位;操作不規范,親人兩行淚!”下列實驗操作不規范的是( )
A.  測定pHB.
測定pHB. 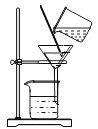 過濾
過濾
C.  蒸發D.
蒸發D. 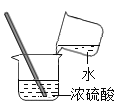 稀釋濃硫酸
稀釋濃硫酸
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請根據所學的化學知識填空:
(1)在抗震救災中,國家給救援人員配備了活性炭口罩,活性炭起_____作用。
(2)生活中常用_____來區別硬水和軟水。
(3)配制500g溶質的質量分數為10%的葡萄糖溶液,主要步驟有:計算、稱量、量取、_____。
(4)我國第一艘國產航母下水,該航母采用了大量鋼鐵作為原材料。鋼鐵生銹的條件是鐵與_____(填化學式)接觸;工業上用赤鐵礦和一氧化碳在高溫條件下來煉鐵,請寫出該反應的化學方程式:_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列圖象能夠正確反映其對應變化關系的是( )
A. 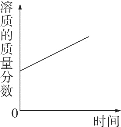 將濃鹽酸露置在空氣中一段時間
將濃鹽酸露置在空氣中一段時間
B. 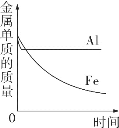 等質量的鋁片、鐵片分別置于潮濕的空氣中
等質量的鋁片、鐵片分別置于潮濕的空氣中
C. 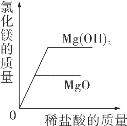 向等質量的氧化鎂、氫氧化鎂中,分別加入質量分數相同的稀鹽酸至過量
向等質量的氧化鎂、氫氧化鎂中,分別加入質量分數相同的稀鹽酸至過量
D. 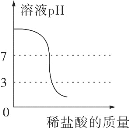 向一定量的氫氧化鈉溶液中滴加pH=3的稀鹽酸
向一定量的氫氧化鈉溶液中滴加pH=3的稀鹽酸
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】高錳酸鉀是錳的重要化合物和常用的氧化劑。以下是實驗室中模擬工業上用軟錳礦制備高錳酸鉀的流程圖。
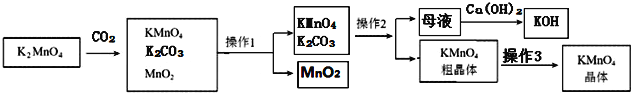
(1)操作1的名稱為_____;該操作中玻璃棒的作用是_____。
(2)寫出流程圖中一種氧化物的化學式_____。
(3)操作3通過降溫結晶法提純高錳酸鉀,屬于____(填“物理”或“化學”)變化。
(4)干燥高錳酸鉀晶體時_____不能太高,原因是_____。實驗室用高錳酸鉀制取氧氣的反應條件為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是居民家用燃氣熱水器示意圖。根據此圖回答:
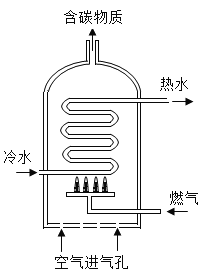
(1)某熱水器以天然氣為燃氣。 若完全燃燒3.2kg的甲烷,則消耗氧氣的質量為______kg。
(2)如下表,1kg三種不同燃料燃燒產生CO2和SO2的質量。由表中數據可知,天然氣是比煤更清潔的能源,原因是______。
燃料 | 燃燒產物質量/g | |
CO2 | SO2 | |
汽油 | 2900 | 5.0 |
天然氣 | 2500 | 0.1 |
煤 | 2500 | 11.0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com