
【題目】.為測定某石灰石樣品中碳酸鈣的質量分數,某同學取30g石灰石樣品,把200g稀鹽酸逐次加入其中,實驗數據如下:
第一次 | 第二次 | 第三次 | 第四次 | |
稀鹽酸質量/g | 50g | 50g | 50g | 50g |
余下固體質量/g | 20g | 10g | 9g | 9g |
試求:(1)此石灰石樣品的純度。(2)200g稀鹽酸中所含氯化氫的質量。
【答案】(1)石灰石樣品的純度為70%;
(2) 200g稀鹽酸中所含氯化氫的質量為29.2g。
【解析】解:(1)分析表中數據可得,石灰石樣品中碳酸鈣的質量=30g-9g=21g,則:石灰石樣品的純度=![]() 100%=70%;
100%=70%;
(2)由表中數據可得,在第一次、第二次實驗中碳酸鈣的質量過量,可按第一次計算,所以在第一次實驗中參加反應碳酸鈣的質量為:30g-20g=10g;
設50g鹽酸中氯化氫的質量為x,
CaCO3 + 2HCl=CaCl2 + H2O + CO2↑
100 73
10g x
![]()
x=7.3g,
則200g稀鹽酸中所含氯化氫的質量:7.3g![]() 4=29.2g;
4=29.2g;
答:(1)石灰石樣品的純度為70%;
(2) 200g稀鹽酸中所含氯化氫的質量為29.2g。


 輕松課堂單元測試AB卷系列答案
輕松課堂單元測試AB卷系列答案 小題狂做系列答案
小題狂做系列答案科目:初中化學 來源: 題型:
【題目】請根據下列實驗裝置圖回答有關問題:
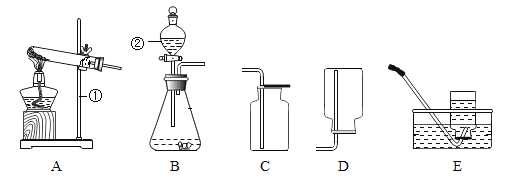
(1)寫出標號儀器的名稱:①________,②________。
(2)用AE組合制取氧氣,有關反應的化學方程式為___________;在氣體收集完畢后,接下來的操作是__________。
(3)實驗室制取二氧化碳用稀鹽酸而不是濃鹽酸,是因為濃鹽酸具有______。常用石灰水檢驗二氧化碳氣體,有關反應的化學方程式是___________。
(4)乙炔是一種微溶于水的氣體,密度與空氣接近,實驗室常用塊狀電石和水在常溫下反應制取乙炔。制取乙炔的發生裝置選_____,收集裝置選_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖為A、B、C三種物質的溶解度曲線,試回答:
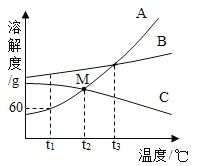
(1)t1℃時A、B、C三種物質的溶解度大小關系是________;。
(2)M點的含義是___________;
(3)t1℃時將40gA物質加入到50g水中充分攪拌,形成溶液的溶質質量分數是___________。
(4)將t3℃時A、B、C三種物質的飽和溶液降溫到t1℃,所得溶液的溶質質量分數大小關系是______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】用化學符號表示:
(1)兩個氦原子 _____
(2)3個氯分子 _____
(3)硝酸根離子 _____
(4)+2價的鎂元素 _____
(5)硫酸鋁 _____
(6)氯化亞鐵 _____
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】益陽市桃江縣硫鐵礦廠開采的黃鐵礦(主要成分是FeS2),是生產H2SO4的重要原料.利用黃鐵礦生產H2SO4的第一步反應為:4FeS2+11O2═2Fe2O3+8X.所得產物Fe2O3是冶煉鐵的重要原料.回答下列問題:
(1)已知FeS2中Fe的化合價為+2,則S的化合價為________.
(2)X的化學式是_________.
(3)寫出高爐中Fe2O3轉化成鐵的化學方程式__________________________.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請按照要求寫出下列反應的化學方程式
(1)有二氧化碳生成的化合反應__________________________________________
(2)有二氧化碳生成的分解反應__________________________________________
(3)有二氧化碳參加的化合反應__________________________________________
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知在常溫下A為液體,B、C、F是氣體; 其中C是最輕的氣體,F是造成溫室效應的主要氣體;G為黑色固體單質,H是白色不溶于水的固體,它們之間的轉變關系如圖,請回答下列問題:
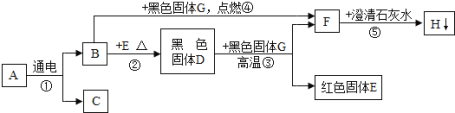
(1)寫出有關物質的化學式:C是 ;G是 ;H是 。
(2)寫出反應②的化學方程式 ,該反應的基本反應類型是 。
(3)寫出反應③的化學方程式: 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列化學方程式能正確表示所述內容的是
A.鐵片入到稀硫酸:2Fe+3H2SO4=Fe2(SO4)3 + 3H2↑
B.氫氧化鈉變質:2NaOH + CO2 = Na2CO3 + H2O
C.實驗室制備CO2:CaCO3 高溫 CaO+CO2↑
D.鐵絲在氧氣中燃燒:4Fe + 3O2 點燃 2Fe2O3
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】金屬的研究、利用對于人類社會有著重要意義.
(1)焊錫是錫鉛合金,把鉛加入錫中制成合金的主要目的是_________.
(2)鋁制品表面易形成致密氧化鋁薄膜,從而阻止鋁進一步被空氣氧化,但氧化鋁能溶于酸.寫出氧化鋁與稀硫酸反應的化學方程式____________________.
(3)把裝滿氯氣的集氣瓶倒扣于加熱至熔化的金屬鈉上,可觀察到的現象是_________________,該反應的化學方程式是_____________________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com