
【題目】人們的日常生活離不開金屬,高科技新材料的開發和應用也需要金屬.
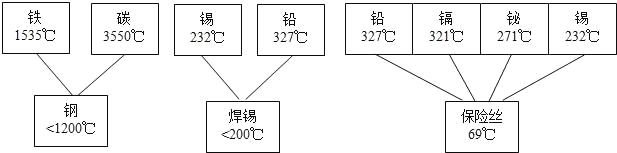
(1)日常使用的金屬材料多數屬于合金.現有一些合金及其組成的純金屬的熔點如圖所示.從圖中數據可以得出結論是:_____.
(2)鋼鐵與潮濕的空氣直接接觸容易生銹造成損失,可采取_____(寫出一種)等措施防止鋼鐵生銹.
(3)人們每年要從金屬礦物資源中提取數以億噸計的金屬.如從鐵礦石(主要成分是氧化鐵)中冶煉出鋼鐵,請你寫出以CO為還原劑的煉鐵化學方程式_____.
 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:初中化學 來源: 題型:
【題目】今年,我國西南地區遭遇了百年不遇的特大旱災,全國人民眾志成城,共抗大旱.
(1)抗旱首先要節約用水,下列做法與節約用水不相符的是___(填序號)
A 農業上推廣使用滴灌技術
B 洗衣、洗菜、淘米水用來澆花、拖地、沖廁所
C 任由水龍頭漏水而不及時修理
D 關停一些污染大、用水量大、產能低的工廠
(2)人工降雨對抗旱發揮了很大作用.常用的人工降雨劑有碘化銀(AgI)和干冰.碘化銀屬于___(填“酸”、“堿”、“鹽”或“氧化物”),干冰用于人工降雨主要是利用干冰升華時會___(填“吸收”或“放出”)大量熱.
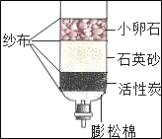
(3)如圖是某同學自制的簡易凈水裝置.其中石英砂的作用是___,起吸附作用的是___.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖為A、B、C三種固體物質的溶解度曲線。
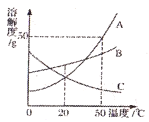
(1)20℃時,三種物質的溶解度大小關系為_____;
(2)50℃時,把50gA物質放入100g水中,充分攪拌,所得溶液是_____(填“飽和”或“不飽和”)溶液,該溶液中溶質質量分數為_____。
(3)20℃時,將接近飽和的B溶液變為飽和溶液,可采用_____方法。
(4)若將C的飽和溶液從50℃降溫到20℃時,發生改變的是_____。
a溶劑質量 b溶質質量 c溶質質量分數 d溶解度
查看答案和解析>>
科目:初中化學 來源: 題型:
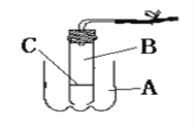
【題目】實驗室用下圖裝置來制取氧氣,請按要求填寫;
(1)寫出圖中有標號的儀器的名稱
①_______②_______③_____________④_____________

(2)用帶導管的橡皮塞塞住試管口,把導管的一端浸在水里,兩手緊貼其外壁,此項操作的目的是__________________________________________。
(3)若用高錳酸鉀來制取氧氣時,則要將一團棉花放在試管口的地方,此項操作的目的是___________________________________________。
(4)只有加熱到氣泡連續地并比較均勻地放出時,才能收集氧氣,原因是_____________________________ 。
(5)收集完畢氧氣后,先要___________,然后再__________________。
(6)如果用向上排空氣法收集時,如何證明該瓶內的氧氣已滿:___________________________;
(7)實驗室高錳酸鉀制氧氣應選用的發生裝置是_____,收集裝置_________。
(8)實驗室用雙氧水制取并且收集得較純氧氣時應選用的發生裝置是______,收集裝置為________。用化學式表示化學反應式__________________________.
(9)實驗室用氯化銨與熟石灰兩種固體加熱制取氨氣,氨氣的密度比空氣小,極易溶于水。推斷:實驗室制取氨氣應選用的發生裝置為_____,收集裝置為____。
(10)利用廢棄的可樂瓶和底部有小孔的試管組成制取氧氣的裝置,該裝置A應盛放__________,B處應放進____________,C是用帶小孔的塑料片。放置C以后使該裝置具有_________________________________________________優點。若使正在發生的反應停止,可以通過操作____________來實現,可看到的現象是_______________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】普通黃銅僅由銅和鋅組成,廣泛用于制造板材、管材等,也用于鑄造機械零件。現有一塊50.00g黃銅樣品,某同學利用一種未知濃度的稀鹽酸來測定樣品中Cu的質量分數。有關數據如圖。問:
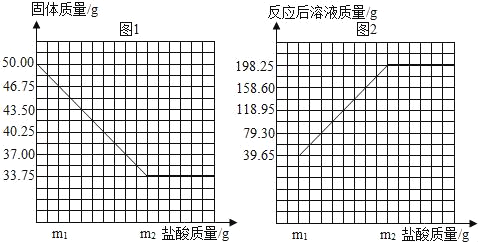
(1)黃銅中Cu的質量分數。
(2)樣品完全反應產生的H2的質量。
(3)稀鹽酸的溶質質量分數。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】綠礬被廣泛用于醫藥和工業領域。工業上利用黃銅礦粉(含雜質)主要成分為CuFeS2制取綠礬(FeSO4·7H2O)的流程圖如下
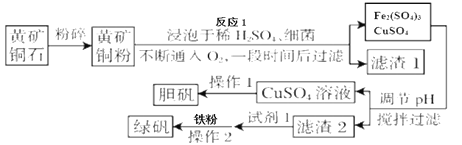
(相關資料)
①氫氧化亞鐵不穩定,在空氣中容易被氧氣氧化成氫氧化鐵。
②三價鐵離子能和金屬鐵反應,方程式為:Fe2(SO4)3 + Fe = 3FeSO4
③FeSO4易溶于水但不溶于乙醇。
④部分陽離子以氫氧化物形式完全沉淀時溶液的pH見下表。
沉淀物 | 開始沉淀pH | 沉淀完全pH |
Cu(OH)2 | 4.2 | 6.7 |
Fe(OH)2 | 7.6 | 9.7 |
Fe(OH)3 | 1.5 | 2.8 |
(問題解答)
(1)將黃銅礦粉粹的目的是____________。
(2)在調節pH時,為了將濾渣2充分轉化為沉淀而析出,需要調節溶液pH的范圍為____________。在調節pH時常用鐵的氧化物來調節,不選用NaOH溶液進行調節,理由是_______。
(3)最后得到的綠礬晶體用乙醇洗滌,不用水進行洗滌的目的是_______。
(4)黃銅礦粉能夠在細菌作用下,與硫酸和氧氣發生反應,請寫出反應1的化學方程式_______
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】鐵及其化合物在生產生活中應用廣泛。
(一)鐵的化合物制備
用廢鐵屑制備鐵紅( 主要成分為 Fe2O3)和 K2SO4 的部分流程如下圖所示:
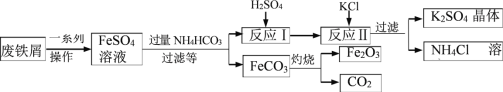
(1)加過量 NH4HCO3 反應時溫度不宜過高的原因為 _____。
(2)反應Ⅰ生成的氣體化學式是 _____;K2SO4 和 NH4Cl 在農業生產中都可做 _____。
(3)為檢驗 K2SO4 中是否混有 Cl-,要先加入足量 _____溶液,靜置后再加向上層清液中滴加少量 _____溶液。
(4)在空氣中灼燒 FeCO3 的化學方程式為 _____。
(二)鐵的冶煉和探究
取 29.0g Fe2O3 粉末,小組同學用下圖裝置模擬煉鐵,并測定反應后固體成分。
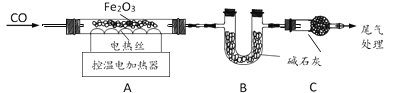
資料:堿石灰可吸收 H2O 和 CO2。
(1)連接裝置,先______,再裝入藥品。
(2)實驗時先通入 CO,目的是______。
(3)通過測定裝置B 中固體質量變化情況,可求得A 中剩余固體質量,裝置C 的作用是______。
(4)現直接測得裝置A 中剩余固體質量為 21.0g,則裝置 B 中固體應增重______g。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在一支試管中放入一小段鎂條(已擦去氧化膜),再向試管中加入一定量的鹽酸,鎂條表面有________產生,反應的化學方程式是________________________________________________________。
[發現問題]為了再次觀察上述反應現象,小林同學用較長的鎂條重做上述實驗,但發現了異常現象,試管中出現了白色沉淀。
[實驗驗證1]小林同學針對兩次實驗的不同,設計對比實驗方案,探究出現異常現象的原因。
試管(盛有同體積同濃度的鹽酸) | ① | ② | ③ | ④ |
鎂條長度 | 1cm | 2cm | 3cm | 4cm |
相同的實驗現象(省略題干現象) | 快速反應,試管發熱,鎂條全部消失 | |||
沉淀量差異(恢復至20℃) | 無 | 少量 | 較多 | 很多 |
[得出結論]鎂條與鹽酸反應產生白色沉淀與________有關。
[追問]白色沉淀是什么物質?
[查閱資料]①20 ℃時,100 g水中最多能溶解氯化鎂54.8 g;
②鎂能與熱水反應產生一種堿和氫氣;
③氯化銀既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:鎂;猜想二:氯化鎂;猜想三:氫氧化鎂,猜想的依據是____________________(用化學方程式表示)。
[實驗驗證2]將白色沉淀洗滌干凈,分別取少量沉淀于A、B、C試管中,進行如表實驗:
試管 | 操作 | 現象 | 結論 |
A | 加入足量鹽酸 | ________,白色沉淀________ | 猜想一不正確,但這種白色沉淀能溶于鹽酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正確 |
C | 加入適量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的離子是: |
繼續滴加幾滴硝酸銀溶液 | 出現大量白色沉淀 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com