
【題目】(題文)(題文)根據鋁與硫酸銅溶液反應的示意圖,請用化學用語表示下列帶點文字部分:
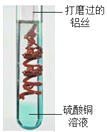
(1)鋁絲進行打磨的目的是除去其表面的氧化鋁簿膜_______;
(2)硫酸銅溶液顯藍色,是因為溶液中含有銅離子____________;
(3)圖中發生反應的化學方程式______________。
科目:初中化學 來源: 題型:
【題目】根據下圖判斷,下列說法錯誤的是( )
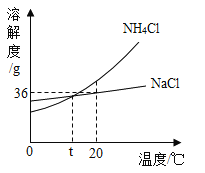
A. NaCl和NH4Cl的溶解度都隨溫度升高而增大
B. 將20℃時某NH4Cl溶液降溫到0℃,其溶質質量分數一定減小
C. 20℃時,20gNaCl加入到50g水中,攪拌后不能全部溶解
D. t℃時,NH4Cl飽和溶液和NaCl飽和溶液溶質質量分數相等
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在硫酸與硫酸銅的混合溶液200g中,滴入40%的NaOH溶液100g,恰好完全反應,記錄反應過程,得到的沉淀與所加的氫氧化鈉溶液的質量關系如圖所示.

回答:
(1)與硫酸銅反應的氫氧化鈉溶液的質量為__________g。
(2)此硫酸的溶質質量分數為________?
(3)反應后溶液溶質的質量分數是_________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】硫酸鋅可作為食品添加劑。工業上常用菱鋅礦生產硫酸鋅,菱鋅礦的主要成分是ZnCO3,并含少量的FeO、CuO。工藝流程圖如下:(假設每一步驟反應均完全)

⑴為提高礦石的溶解速度,操作1是___________ 。
⑵菱鋅礦溶解后所得的溶液中金屬陽離子有_____________種。
⑶反應1中H2O2轉化為H2O,同時有Fe2(SO4)3生成,寫出反應1中生成Fe2(SO4)3的化學方程式___________________________。
⑷結晶之前,溶液中除了硫酸鋅,還一定存在的溶質是_________________。
⑸硫酸鋅晶體的溶解度曲線如下圖所示,若要獲得ZnSO4·7H2O晶體,應控制結晶時的溫度范圍為____________________。

⑹流程中還可能得到一種紫羅蘭色晶體(NH4)xFey(SO4)z·7H2O。已知該化合物中氮、鐵元素質量比為1:4,則x:y :z=________
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列應用和相應的化學方程式都正確的是
A. 高爐煉鐵發生的主要反應:2Fe2O3+3C高溫4Fe+3CO2↑
B. 用生石灰處理硫酸廠廢液:Ca(OH)2+H2SO4=CaSO4+2H2O
C. 用硝酸銀溶液鑒別海水和蒸餾水:AgNO3+NaCl=AgCl↓+NaNO3
D. 用稀鹽酸鑒別黃銅和黃金:Cu + 2HCl = CuCl 2 + H2↑
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】MnO2是一種既不溶于水也不溶于稀硫酸的重要無機功能材料,粗MnO2(含有較多的MnO和MnCO3)的提純是工業生產的重要環節。下圖是某研究性學習小組在實驗室中模擬工業上粗MnO2轉化為純MnO2的工藝流程。

請回答下列問題:
(1)操作A的名稱是_____;蒸發操作中玻璃棒的作用是____;
(2)NaClO3中氯元素的化合價為____________價;
(3)寫出粗MnO2樣品加稀H2SO4時產生CO2的化學方程式________;
(4)該流程中可以循環利用的物質是H2SO4和________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】結合如圖所示驗證氫氧化鈣化學性質的實驗圖示,回答有關問題.
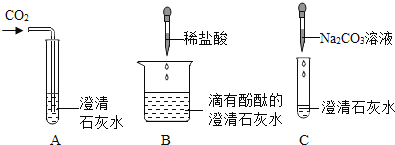
(1)實驗A中,一定能夠觀察到的明顯現象是________;
(2)實驗B驗證了氫氧化鈣能跟酸、_______作用;
(3)實驗C中發生的反應可用化學方程式表示為_______________;
(4)已知Na2CO3溶液呈堿性,將A、B、C三個實驗后的所有物質倒入同一個燒杯中,發現有氣泡產生,最后只得到了無色溶液,則最后得到的無色溶液中一定含有的溶質是____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】科學家發現,通過簡單的化學反應,可以將樹木的纖維素變成超級儲能裝置,下圖是該反應的微觀示意圖,下列說法正確的是________
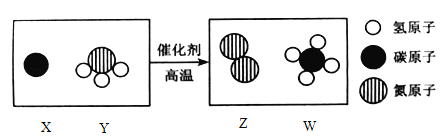
A.W物質中碳元素的質量分數為50%
B.化學反應前后原子的種類、個數、質量均保持不變
C.上圖中涉及的化合物有3種
D.參加該反應中Z與W的分子個數比為__________
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】CaCO3在生產生活中有廣泛的用途.
(1)煅燒石灰石可制得活性CaO,反應的化學方程式為___________。為測定不同煅燒溫度對CaO活性的影響,某化學興趣小組進行了如下實驗:
Ⅰ.取石灰石樣品分為三等份,在同一設備中分別于800℃、900 ℃和1000℃條件下煅燒;
Ⅱ.所得固體分別與等質量的水完全反應,測得反應液溫度隨時間的變化如圖1所示。上述溫度中,___________℃時煅燒所得CaO活性最高。
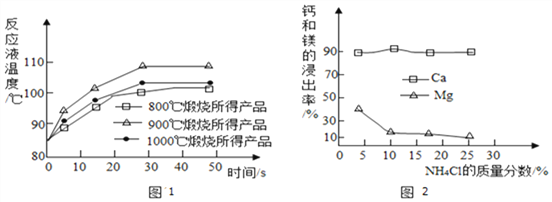
(2)以電石渣(主要成分為Ca(OH)2,還含有少量MgO等雜質)為原料制備高純活性CaCO3的流程如圖3。(資料:氨水的pH約為11.7,氫氧化鎂完全沉淀的pH約為10.87)
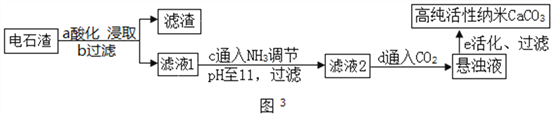
①步驟a中加入的藥品為NH4Cl溶液,由此說明NH4Cl溶液呈________性(填酸性、中性或堿性);如圖2為濃度對鈣、鎂元素浸出率的影響。由圖可知NH4Cl溶液的質量分數達到10%以上主要溶解的是Ca(OH)2;浸取時主要發生反應的化學方程式為_________________。
②流程c通入NH3的目的主要有兩個,一是調節溶液的pH值,二是_______。
③濾液1中通入NH3和CO2后生成碳酸鈣和氯化銨,寫出發生反應的化學方程式為________________。
④向濾液1中滴加Na2CO3溶液,也能得到CaCO3,從節約藥品角度分析圖3所示流程中可循環利用的物質有__________________(寫出兩種物質)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com