
【題目】為了對KCl樣品(含少量KNO3)進行分組分析,甲、乙、丙三位同學分別進行實驗,他們實驗數據如下表,請仔細觀察和分析數據回答問題:(已知KCl+AgNO3=KNO3+AgCl↓)
甲 | 乙 | 丙 | |
所取固體樣品的質量/g | 20 | 10 | 10 |
加入AgNO3溶液的質量/g | 100 | 100 | 150 |
反應后所得沉淀的質量/g | 14.35 | 14.35 | 14.35 |
⑴三位同學中_____同學所用KCl和AgNO3恰好完全反應(填編號)。
⑵樣品中KCl的質量分數是多少?_____
⑶三位同學分別把反應后的溶液過濾,哪一位同學所得的溶液是只含有一種溶質的溶液?_______此溶液中溶質的質量分數是多少?_____
【答案】乙 74.5% 乙 13.2%
【解析】
(1)由甲和乙反應的數據可知,甲中氯化鉀過量,由乙和丙反應的數據可知,丙中硝酸銀過量,因此乙中的氯化鉀和硝酸銀恰好完全反應;
(2)設:樣品中氯化鉀的質量為x,反應生成的硝酸鉀質量為y。
![]()
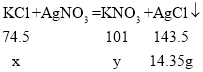
![]() x=7.45g
x=7.45g
![]() y=10.1g
y=10.1g
樣品中氯化鉀的質量分數=![]() ;
;
答:樣品中氯化鉀的質量分數是74.5%。
(3)甲同學得到的溶液中,含有的溶質是硝酸鉀和氯化鉀,硝酸鉀包括樣品中的硝酸鉀和反應生成的硝酸鉀,氯化鉀是過量剩余的氯化鉀;丙同學得到的溶液中,含有硝酸鉀和硝酸銀,硝酸鉀包括樣品中的硝酸鉀和反應生成的硝酸鉀,硝酸銀是過量剩余的硝酸銀;
乙同學得到的溶液中,只含有硝酸鉀,包括樣品中的硝酸鉀和反應生成的硝酸鉀,由(2)計算可知,反應生成的硝酸鉀為10.1g,10g樣品中,硝酸鉀的質量為:10g-7.45g=2.55g,
則最后所得溶液中,溶質硝酸鉀的質量=10.1g+2.55g=12.65g,溶液質量=10g+100g-14.35g=95.65g;此溶液中溶質的質量分數為:![]() 。
。
答:乙同學所得的溶液是只含有一種溶質的溶液,此溶液中溶質的質量分數為13.2%。


科目:初中化學 來源: 題型:
【題目】如圖是初中化學中常見的實驗。
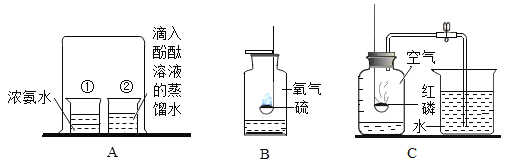
(1)A中現象:燒杯②中溶液變紅。請用分子的知識解釋“變紅”的原因_________。
(2)B中集氣瓶底部有少量水,其作用是 ______。
(3)C實驗完畢,集氣瓶內水面上升到一定高度后,不能繼續上升,這種現象說明氮氣具有______的性質;若從燒杯中進入集氣瓶內水的體積明顯小于瓶內原空氣體積的五分之一,可能存在的原因是______。(寫出一條即可)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】置換反應是中學化學反應的基本反應類型之一.
已知:化合物A+單質B→化合物C+單質D.試回答下列問題.
(1)若D為氫氣,A為稀硫酸,則B應滿足的條件是____________.
(2)若D為銅,化合物A的化學式可能為____________.
(3)已知在高溫條件下碳與水蒸氣可反應生成一氧化碳和氫氣(水煤氣的主要成分),寫出該反應的化學方程式____________.若家中發生燃氣(天然氣)泄漏,
下列措施不可行的是_____(填字母序號)。
A.檢查并關閉氣源閥門 B.輕輕打開門窗通風 C.立即打開抽油煙機排氣
(4)非金屬單質也具有類似金屬與金屬化合物溶液之間發生置換反應的規律,即活動性較強的非金屬可把活動性較弱的非金屬從其化合物溶液中置換出來,如在溶液中可發生下列反應:
Cl2+2NaBr═2NaCl+Br2、I2+Na2S═2NaI+S↓、Br2+2KI═2KBr+I2
由此判斷S、Cl2、I2、Br2四種單質中非金屬活動性最強的是______,最弱的是____________.
(5)在化學反應中,物質所含元素的化合價發生變化的反應就是氧化還原反應,據此判斷置換反應____________填“屬于”或“不屬于”)氧化還原反應.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在t℃時,濃度相同的兩份KNO3溶液A和B,A為100g,B為80g,將其各自恒溫蒸發掉20g水后,A剛好飽和,對所得的B溶液正確的說法是 ( )
A. 也剛好飽和 B. 仍為不飽和溶液
C. 是飽和溶液并有晶體析出 D. 有晶體析出但溶液仍為不飽和溶液
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】學校研究性學習小組為了測定當地礦山石灰石中碳酸鈣的質量分數,取來了一些礦石樣品,并取稀鹽酸200 g,平均分成4份進行實驗,結果如下:
實驗 | 一 | 二 | 三 | 四 |
加入樣品的質量/g | 5 | 10 | 15 | 20 |
生成的CO2質量/g | 1.76 | 3.52 | 4.4 | m |
(1)上表中m的數值是 ;
(2)反應中礦石有剩余是第 次實驗;
(3)這種石灰石礦中碳酸鈣的質量分數是 ;
(4)稀鹽酸中溶質的質量分數是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列是初中化學常見的實驗。請回答下列問題
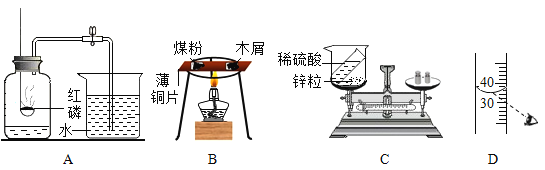
(1)圖A所示實驗結束后,進入集氣瓶中水的體積小于瓶內原氣體體積的五分之一,造成該現象的原因是_____(答出一條即可)。
(2)圖B所示實驗觀察到木屑先燃燒,燃燒的順序說明燃燒的條件之一是_____。
(3)圖C所示實驗不能驗證質量守恒定律的原因是_____。
(4)配制一定質量分數的氯化鈉溶液,按圖D所示量取溶劑,其他操作均正確,最終導致配制的溶液溶質的質量分數_____(填“偏大”、“偏小”或“不變”)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】閱讀下面二氧化硫的相關信息,并回答問題:
二氧化硫是無色、有刺激性氣味的氣體,密度比空氣大,容易液化,易溶于水。二氧化硫與水反應生成亞硫酸(H2SO3),溶液顯酸性。亞硫酸不穩定,容易分解成水和二氧化硫。二氧化硫在一定條件下,可以被氧氣氧化成三氧化硫。實驗室通常用亞硫酸鈉(Na2SO3)和70%的硫酸反應來制取二氧化硫。
(1)通過以上信息可知二氧化硫的化學性質有_____(答出一條即可)
(2)二氧化硫和二氧化碳既有相似性,又有差異性。通過以下實驗進行比較:
實驗一:在水槽中滴入紫色石蕊溶液將收集滿兩種氣體的試管同時倒立于其中,一段時間后實驗現象如圖所示,同時觀察到左側試管內溶液變紅,右側試管內溶液_____(填“變紅”或“不變紅”)。該實驗說明相同條件下二氧化硫的溶解性_____(填“大于”或“小于”)二氧化碳的溶解性。
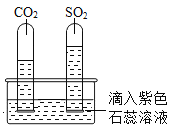
實驗二:將少量二氧化碳和二氧化硫分別通入澄清石灰水中,都出現白色渾濁。請用化學方程式解釋二氧化硫使澄清石灰水變渾濁的原因:_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A~F是初中化學中常見的物質。A、C是碳的兩種氧化物,B是紅棕色的粉末,D是年產量最高的金屬。物質間的相互關系如圖(“一”表示兩端的物質能發生反應,“→”表示一種物質在一定條件下能轉化為另一種物質。部分反應物生成物和反應條件已略去)。請回答:
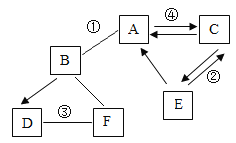
(1)反應①的化學方程式為_____。
(2)反應②由C→E的轉化在自然界中可通過_____實現。
(3)如果F為稀硫酸反應③所得溶液中一定含有的溶質是_____(填物質名稱),該反應的基本反應類型是_____。
(4)反應④的化學方程式:_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖所示為實驗室常用的實驗裝置:
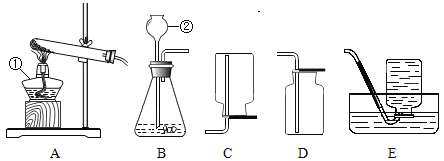
據此回答下列問題:
(1)寫出帶標號儀器的名稱:①_____②_____.
(2)常溫下,在過氧化氫(H2O2)溶液中加入MnO2(固體粉末)即可制取氧氣。用這種方法制取氧氣時,應選用的發生裝置是_____(填序號),選擇依據是_____和_____。
(3)實驗室通常用_____和_____反應制取CO2,該反應的化學方程式_____;此外,CO2可以用碳酸氫鈉粉末(NaHCO3)加熱分解(產物為碳酸鈉、二氧化碳和水)來制取,選擇的制取裝置為_____,該反應的化學方程式為:_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com