
【題目】食鹽、碳酸鈉和碳酸氫鈉是生活中常見的鈉鹽。請回答下列問題。
(1)碳酸氫鈉的水溶液顯_____性(填“酸”、“堿”或“中”)。碳酸氫鈣受熱易分解,碳酸氫鈉性質(zhì)與其相似,除去碳酸鈉固體中混有的少量碳酸氫鈉,反應的化學方程式為_______________________________。
(2)等質(zhì)量的碳酸鈉和碳酸氫鈉分別與足量鹽酸反應時生成的CO2量,前者_____后者(填“>”、“<”或“=”)。
(3)粗鹽含有少量雜質(zhì)(主要為CaCl2、MgCl2、Na2SO4等)。用粗鹽制取“化學純”級的NaCl,步驟為溶解、加過量a、加過量NaOH、加過量b、過濾、加適量鹽酸,蒸發(fā)結晶得到“化學純”級的NaCl固體。試劑a、b分別是_____(填序號)
A Na2CO3、BaCl2 B BaCl2、Na2CO3 C BaCl2、Na2SO4
(4)工業(yè)上用電解飽和食鹽水的方法生成氯氣和燒堿。
資料一:Cl2+H2O=HCl+HClO
資料二:初中化學中,我們學習了酸和堿發(fā)生中和反應的實質(zhì)是H++OH﹣=H2O,像這種用實際參加反應的離子符號來表示反應的式子叫離子反應,離子方程式的書寫一般按以下步驟:(以Na2SO4與BaCl2反應為例)
①寫出Na2SO4與BaCl2反應的化學方程式:_________________________
②把易溶于水,易電解的物質(zhì)寫成離子形式,把難溶的物質(zhì)、氣體和水等仍用化學式表示,上述化學方程式可改寫成,2Na++SO42﹣+Ba2++2Cl﹣=BaSO4↓+2Na++2Cl﹣
③刪去方程兩邊不參加反應的離子:Ba2++SO42﹣=BaSO4↓:
④檢查方程式兩邊各元素的原子個數(shù)和電荷總數(shù)是否相等
⑤某化工廠發(fā)生氯氣泄漏事件,工作人員噴射NaOH溶液形成液幕,包圍并吸收泄漏的氯氣,其反應原理________________________(用離子方程式表示)
資料三:化學反應類型有不同的分法,其中反應前后,有元素化合價變化的化學反應是氧化還原反應。氧化還原反應中有元素化合價升高的反應物是還原劑,有元素化合價降低的反應物是氧化劑,化合價沒有發(fā)生變化的既不是氧化劑也不是還原劑。
⑥工業(yè)上可用氨檢驗輸送氯氣的管道是否漏氣。反應方程式如下:8NH3+3Cl2=6NH4Cl+N2,該反應_____(填“是”或“不是”)氧化還原反應,其中氧化劑和還原劑物質(zhì)的量之比為__________(若是氧化還原反應,此空作答,反之,不作答)
【答案】堿 2NaHCO3![]() Na2CO3+H2O+CO2↑ < B BaCl2+Na2SO4═BaSO4↓+2NaCl Cl2+2OH﹣=Cl﹣+ClO﹣+H2O 是 3:2
Na2CO3+H2O+CO2↑ < B BaCl2+Na2SO4═BaSO4↓+2NaCl Cl2+2OH﹣=Cl﹣+ClO﹣+H2O 是 3:2
【解析】
(1)碳酸氫鈉的水溶液顯堿性,碳酸氫鈣受熱易分解,碳酸氫鈉性質(zhì)與其相似,除去碳酸鈉固體中混有的少量碳酸氫鈉,可以將固體混合物充分加熱,反應的化學方程式為2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(2)碳酸鈉和碳酸氫鈉與鹽酸反應生成二氧化碳的關系式為:![]() 、
、![]() ,可知等質(zhì)量的碳酸鈉和碳酸氫鈉分別與足量鹽酸反應時生成的CO2量,前者<后者;
,可知等質(zhì)量的碳酸鈉和碳酸氫鈉分別與足量鹽酸反應時生成的CO2量,前者<后者;
(3)粗鹽含有少量雜質(zhì)(主要為CaCl2、MgCl2、Na2SO4等)。用粗鹽制取“化學純”級的NaCl,為將雜質(zhì)離子除盡,所加試劑要過量,過量的試劑,在后續(xù)操作中必須除去;可用氫氧化鈉除去鎂離子,用氯化鋇除去硫酸根,用碳酸鈉除去鈣離子及過量的鋇離子,實驗步驟為溶解、加過量BaCl2、加過量NaOH、加過量Na2CO3、過濾、加適量鹽酸,蒸發(fā)結晶得到“化學純”級的NaCl固體。選B;
(4)①氯氣與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水,離子方程式為Cl2+ 2OH-=Cl-+ ClO-+ H2O;
②反應前后,有元素化合價變化的化學反應是氧化還原反應。氧化還原反應中有元素化合價升高的反應物是還原劑,有元素化合價降低的反應物是氧化劑,化合價沒有發(fā)生變化的既不是氧化劑也不是還原劑。工業(yè)上可用氨檢驗輸送氯氣的管道是否漏氣。該反應中,氯元素的化合價降低,被還原;氯氣作氧化劑,氨氣中氮元素的化合價升高,被氧化,氨氣作還原劑,參加的氨氣中只有2個分子氨氣被氧化,物質(zhì)的量之比等于分子個數(shù)之比,該反應中氧化劑和還原劑物質(zhì)的量之比為3:2。


科目:初中化學 來源: 題型:
【題目】化學就在我們身邊,化學與我們的生活息息相關。
(1)煤是一種常用的化石燃料,家庭用煤經(jīng)過了從“煤球”到“蜂窩煤”的變化,以前人們把煤粉加工成略大于乒乓球的球體,后來人們把煤粉加工成圓柱體,并在圓柱體內(nèi)打上一些孔(如圖).請你分析這種變化的優(yōu)點是:_____。

(2)為了全民的健康,衛(wèi)生部推廣使用強化加鐵醬油.這里的“鐵”指的是_____(填“單質(zhì)”“元素”或“原子”)。
(3)熟石灰是松散的粉末,將它調(diào)成石灰漿抹墻,一段時間后,墻面變得潔白而堅固且會“出汗”請寫出有關的化學方程式_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現(xiàn)有鹽酸和氯化鎂的混合溶液,向其中逐滴滴入氫氧化鈉溶液,生成沉淀質(zhì)量與滴入氫氧化鈉溶液質(zhì)量的變化關系如圖所示。下列說法錯誤的是

A. 滴加氫氧化鈉溶液質(zhì)量為a~cg時,溶液中發(fā)生的反應為:![]()
B. 滴加氫氧化鈉溶液質(zhì)量至ag時,溶液中溶質(zhì)質(zhì)量比原混合溶液中溶質(zhì)質(zhì)量大
C. 滴加氫氧化鈉溶液質(zhì)量至bg時,溶液中含三種溶質(zhì)
D. 滴加氫氧化溶液質(zhì)量至cg時,溶液呈中性
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】CaSO42H2O受熱會逐步失去結晶水.取純凈的CaSO42H2O固體3.44g進行加熱,測定固體質(zhì)量隨溫度的變化情況如圖所示.C點固體的化學式是_____.T3~T4溫度段加熱固體所產(chǎn)生的氣體是形成酸雨的主要物質(zhì)之一,則D~E段發(fā)生反應的化學方程式為_____.

查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】向53g質(zhì)量分數(shù)為10%的碳酸鈉溶液中逐滴加入質(zhì)量分數(shù)為5%的稀鹽酸,生成二氧化碳的質(zhì)量隨加入鹽酸質(zhì)量的變化關系如圖所示.(不考慮CO2的溶解)

已知:
OB段反應的化學方程式為Na2CO3+HCl═NaCl+NaH CO3
BD段(不含B點)反應的化學方程式為NaH CO3+HCl═NaCl+H2O+CO2↑
請回答:
(1)53g質(zhì)量分數(shù)為10%的碳酸鈉溶液中溶質(zhì)質(zhì)量為___________g.
(2)A點對應溶液中溶質(zhì)有_________(填化學式).
(3)B點橫坐標為________(計算結果保留1位小數(shù),下同)
(4)假設C點橫坐標為54.75,計算C點對應的二氧化碳質(zhì)量.(寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在實驗室里加熱氯酸鉀(KClO3)和二氧化錳的混合物制取氧氣,實驗測得試管中固體的質(zhì)量隨時間變化的相關數(shù)據(jù)見下表:請通過計算回答:
加熱時間/min | 0 | t1 | t2 | t3 | t4 |
固體質(zhì)量/g | 28.0 | 25.4 | 23.2 | 18.4 | 18.4 |
請請通過計算回答:
(1)實驗過程中共制得氧氣_____g;
(2)當完全反應后,二氧化錳的質(zhì)量為_____g;
(3)原混合物中氯酸鉀的質(zhì)量分數(shù)___?(寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某實驗小組同學對碳酸鈉和碳酸氫鈉的化學性質(zhì)進行研究。進行如下兩個實驗:
(實驗一)熱穩(wěn)定性。
對碳酸鈉和碳酸氫鈉固體分別加熱發(fā)現(xiàn),二者熱穩(wěn)定性有明顯差異。只有碳酸氫鈉會受熱分解。請寫出發(fā)生的化學反應方程式:___。
(實驗二)與酸的反應
將等質(zhì)量、等濃度的碳酸鈉和碳酸氫鈉溶液分別與相同鹽酸反應,發(fā)現(xiàn)碳酸氫鈉溶液產(chǎn)生氣泡的速率明顯快于碳酸鈉溶液。實驗后大家對碳酸鈉溶液與鹽酸反應后的燒杯中的溶質(zhì)成分發(fā)生了興趣。
(提出問題)該燒杯內(nèi)溶液的溶質(zhì)是什么?
(做出猜想)猜想一:可能是NaCl和HCl:猜想二:可能只有NaCl:猜想三:可能是_____。
(進行實驗)實驗步驟1:
取少量燒杯內(nèi)的溶液于試管中,滴入幾滴酚酞溶液,振蕩,發(fā)現(xiàn)_____;結論:猜想三不正確。
實驗步驟2:
取少量燒杯內(nèi)的溶液于試管中,加入少量硝酸銀溶液,振蕩,產(chǎn)生白色沉淀。結論:溶液中有HCl,猜想二不正確,猜想一正確。
蛋蛋同學認為步驟2不能證明猜想二錯誤,原因是_____。
根據(jù)所學化學知識,你認為可采用下列物質(zhì)中的_____(填字母)來代替實驗步驟2的硝酸銀溶液進一步實驗,從而驗證猜想一和猜想二的正確性。
a.pH試紙 b.鐵粉 c.銅粉 d.氧化銅固體
(反思交流)燒杯中溶液未經(jīng)處理直接倒入下水道,可能造成的危害是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗課上,同學們發(fā)現(xiàn)一瓶久置空氣中的氧化鈉固體的瓶口有白色粉末。在老師指導下,同學們對該白色粉末的成分進行了討論。
(猜想與假設) 猜想I:白色粉末是碳酸鈉
猜想II:白色粉末是氫氧化鈉
猜想III:白色粉末是_____________________
(查閱資料)CaCl2溶液,Ca(NO3)2溶液呈中性。
(實驗探究)取白色粉末溶于水形成溶液A,設計如下實驗:
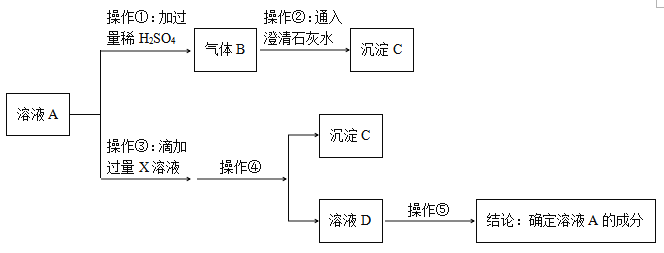
(1)由上述實驗可知,猜想_______肯定不成立。
(2)若操作①滴加過量稀鹽酸有氣體B產(chǎn)生,而滴加少量稀硫酸可能沒有氣體B產(chǎn)生。其可能的原因是:_____________(用化學方程式回答)。
(3)適合操作③的X溶液是_______(填字母序號)。
A. CaCl2溶液 B. Ca(OH)2溶液 C. Ba(OH)2溶液 D. Ca(NO3)2溶液
(4)操作④需要用到的玻璃儀器是______________。
(5)請寫出操作⑤的兩種方案并得出結論。
方案一:________________________________________。
方案二:_________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】右圖是甲、乙、丙三種固體物質(zhì)的溶解度曲線。下列說法不正確的是( )
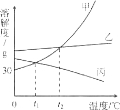
A.在t2℃時,甲、乙兩種物質(zhì)的溶解度相等
B.0℃時,將20g甲物質(zhì)加入50g水中,所得溶液質(zhì)量為70g
C.t1℃時,將丙的飽和溶液升溫至t2℃,有晶體析出
D.在tl℃時,甲的飽和溶溶和丙的飽和溶液中溶質(zhì)的質(zhì)量分數(shù)相同
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com