
【題目】如圖1是實驗室常用氣體制備裝置,據圖回答問題:
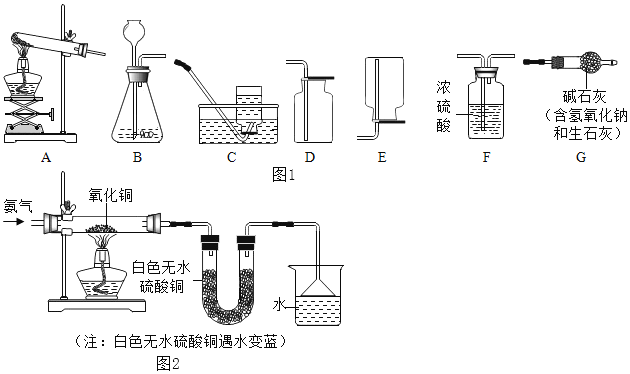
![]() 選擇C裝置收集氧氣是因為______。將帶火星的木炭伸入盛有氧氣的集氣瓶中,實驗現象是______。
選擇C裝置收集氧氣是因為______。將帶火星的木炭伸入盛有氧氣的集氣瓶中,實驗現象是______。
![]() 實驗室制取氨氣:
實驗室制取氨氣:![]() 固
固![]() 固)
固)![]()
![]() 固
固![]() ,要制取并收集干燥的氨氣,所選裝置正確的連接順序是______
,要制取并收集干燥的氨氣,所選裝置正確的連接順序是______![]() ______
______![]() ______
______![]() 填字母代號
填字母代號![]() 。
。
![]() 為探究氨氣的性質,按如圖2裝置進行實驗。觀察到黑色粉末變紅,白色無水硫酸銅變藍,同時反應中還有一種氣體單質生成。
為探究氨氣的性質,按如圖2裝置進行實驗。觀察到黑色粉末變紅,白色無水硫酸銅變藍,同時反應中還有一種氣體單質生成。
(查閱資料)氧化亞銅![]() 是紅色固體,易與稀硫酸反應:
是紅色固體,易與稀硫酸反應:![]() 。
。
(提出問題)得到的紅色物質是什么?
(猜想)①是Cu;②是![]() ;③是______。
;③是______。
若猜想①成立,玻璃管中發生反應的化學方程式為______,說明![]() 具有還原性。
具有還原性。
(設計實驗)請你設計一個簡單的實驗來驗證紅色物質中是否存在![]() :______。
:______。
【答案】氧氣不易溶于水 木炭復燃,發出白光 A G E Cu、![]()
![]() 實驗步驟:取少量紅色固體于試管中,加入足量稀硫酸;實驗現象及結論:如紅色固體部分溶解,溶液變藍,證明紅色物質中有Cu2O,若溶液不變色,則無Cu2O。
實驗步驟:取少量紅色固體于試管中,加入足量稀硫酸;實驗現象及結論:如紅色固體部分溶解,溶液變藍,證明紅色物質中有Cu2O,若溶液不變色,則無Cu2O。
【解析】
(1)氧氣不易溶于水,可用排水法收集;將帶火星的木炭伸入盛有氧氣的集氣瓶中時,木炭復燃,發出白光。
(2)制取氨氣的反應物為固體,反應條件為加熱,故選用A裝置作反應裝置,濃硫酸有酸性,不可用來干燥NH3,應選用G裝置,氨氣的相對分子質量為17,小于空氣的平均值29,因此其密度小于空氣,需采用向下排空氣法收集,故選用E裝置。
(3)等到的紅色物質可能是其中一種,也可能是兩種混合,因此可能是Cu、Cu2O混合物。
若猜想![]() 成立,即生成了Cu,白色無水硫酸銅變藍,證明生成了H2O,根據質量守恒定律可知,另一種氣體單質是由氮元素組成的,即N2,則化學方程式為
成立,即生成了Cu,白色無水硫酸銅變藍,證明生成了H2O,根據質量守恒定律可知,另一種氣體單質是由氮元素組成的,即N2,則化學方程式為![]() 。
。
由題意知,氧化亞銅![]() 是紅色固體,易與稀硫酸反應,化學方程式為
是紅色固體,易與稀硫酸反應,化學方程式為![]() 。可向樣品中加入稀硫酸,通過判斷是否有CuSO4及Cu產生來推斷樣品中有無Cu2O。實驗步驟:取少量紅色固體于試管中,加入足量稀硫酸;實驗現象及結論:如紅色固體部分溶解,溶液變藍,證明紅色物質中有Cu2O,若溶液不變色,則無Cu2O。
。可向樣品中加入稀硫酸,通過判斷是否有CuSO4及Cu產生來推斷樣品中有無Cu2O。實驗步驟:取少量紅色固體于試管中,加入足量稀硫酸;實驗現象及結論:如紅色固體部分溶解,溶液變藍,證明紅色物質中有Cu2O,若溶液不變色,則無Cu2O。


 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:初中化學 來源: 題型:
【題目】如圖是甲、乙兩物質(均不含結晶水)的溶解度曲線,下列說法錯誤的是()

A.甲、乙均屬于易溶性物質
B.10°C時,等質量的甲、乙飽和溶液中所含溶質的質量相等
C.10°C時,分別將甲、乙兩物質的溶液恒溫蒸發等質量的水,析出晶體的質量不一定相等
D.20°C時,乙物質溶液的溶質質量分數約為33.3%
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為了測定某黃銅樣品中銅的質量分數,某化學小組進行了如下實驗:
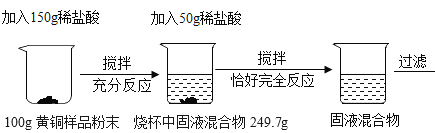
請回答下列問題:
(1)上述實驗過程中發生反應的化學方程式為_____;
(2)根據已知條件列出求解第一次所加的稀鹽酸中溶質質量(x)的比例式_____;
(3)此黃銅樣品中銅的質量分數為_____;
(4)用 36.5%的濃鹽酸配制 200g 上述稀鹽酸,所需濃鹽酸的質量為_____g;
(5)若將反應后的濾液蒸發掉 12.6g 水,所得不飽和溶液中溶質的質量分數為_____;
(6)欲將黃銅樣品中的銅轉化為銅鹽,可將過濾后所得固體洗滌、烘干,然后在空氣中加熱,充分反應,可得到氧化銅的質量是_____g,再經過某些反應及操作就得到了所 需銅鹽。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某研究性學習小組為探究鎂與水的反應,設計如下實驗:
步驟1:將鎂條用砂紙打磨至光亮,分成兩等份.
步驟2:將一份光亮的鎂條置于冷水中,幾乎沒有觀察到任何變化.
步驟3:將另一份光亮的鎂條置于熱水中,觀察到有氣泡產生.
(1)將鎂條用砂紙打磨至光亮的原因是______.
(2)某些活潑金屬與水反應生成對應的堿和氫氣,如果金屬活動性越強,生成的堿的堿性越強.某同學就向步驟3的燒杯中滴加酚酞溶液,觀察到鎂條的周圍有明顯的紅色出現(此時難溶性物質有微量溶解).該反應的化學方程式______.
(3)步驟2和步驟3對比可知,影響鎂與水反應速率的一個因素是______.
(4)根據以上信息,若將金屬鈉加到硫酸銅溶液中,可能觀察到的現象是______.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列是分析久置空氣中的NaOH固體的相關實驗![]() 不考慮水分
不考慮水分![]() ,其中不合理的是
,其中不合理的是![]()
![]()
序號 | 實驗目的 | 實驗方案 |
① | 證明變質 | 取少量固體,加水溶解,滴加足量稀鹽酸,觀察是否有氣泡產生 |
② | 確定成分 | 取少量固體,加入石灰水,過濾,向濾液中滴加酚酞試液 |
③ | 測定純度 | 取ag樣品與足量氯化鋇溶液充分反應,將沉淀過濾、洗滌、干燥,得到mg固體 |
④ | 除去雜質 | 取一定量固體,加水溶解,滴加澄清石灰水至恰好完全反應,過濾 |
A.①B.②C.③D.④
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】做電解水實驗時,常向水中加入稀硫酸以增強導電性,但硫酸并未參加反應。
(1)小明量取40 mL溶質質量分數為34%的硫酸溶液(密度為1.25 g/mL),其中溶質的質量為________g。
(2)將(1)中量取的硫酸溶液加水稀釋成5%的稀硫酸,應加入水的質量為__________g。
(3)取90 g 5%的稀硫酸做電解水實驗,通電一段時間后,收集到氫氣的質量為2 g,求此時溶液中溶質的質量分數_______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】向盛有100g稀硫酸的燒杯中加入一定量的鎂粉,固體完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀質量與加入NaOH溶液的質量關系如圖所示。
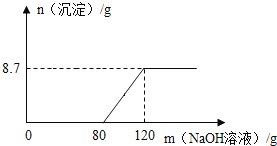
(1)反應生成沉淀的質量為_____克。
(2)鎂粉完全溶解后所得溶液中的溶質成分為_____。
(3)計算氫氧化鈉溶液的溶質質量分數_____(要求寫出計算過程)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A為黑色固體,A、C、D、Y都是氧化物,E是單質,F、G為常見的物質,其中B、E、G屬于單質,如圖是它們之間的相互轉化關系。請回答:
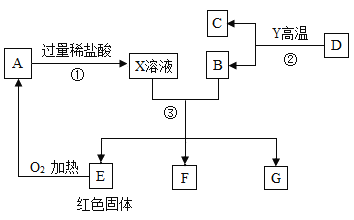
(1)寫出下列物質的化學式:
A:_____ D:_____ Y:_____。
(2)X溶液中所含有的溶質為_____;F溶液所含有的溶質是_____。
(3)寫出下列反應的化學方程式:反應③中生成無色氣體的化學方程式_____。G和A在加熱條件下發生的化學反應的化學方程式_____。
(4)D與Y的反應在_____方面有重要作用。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】欲測定Cu﹣Zn合金及Cu﹣Ag合金中銅的質量分數,實驗室只提供一瓶未標明質量分數的稀硫酸和必要的儀器。
(1)你認為能測出合金中銅的質量分數的是_____合金。
(2)取該合金的粉末32.5g加入該硫酸充分反應,所加稀硫酸與生成的質量關系如圖所示。
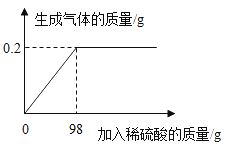
①生成氣體的質量為_____g。
②請計算該合金中銅的質量分數。_____(請在寫出第②問的詳細解答過程)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com