
【題目】繼黃金、白金之后,鈀金(Pd)首飾在市場上悄然興起。為了獲得鈀金,取17.7%的PdCl2溶液100g,加入10.0g鐵粉使其充分反應得鈀金和鐵的氯化物。經分析所得鈀金的質量為10.6g,未反應的鐵粉質量為4.4g,下列說法正確的是( )
A. 生成鐵的氯化物質量為![]() B. 生成鐵的氯化物質量為
B. 生成鐵的氯化物質量為![]()
C. 該反應說明鈀金比鐵活潑D. 生成鐵的氯化物為![]()
 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
【題目】下列實驗操作、現象和結論對應正確的是( )
實驗操作 | 現象 | 結論 | |
A | 向久置于空氣中的NaOH溶液滴加稀H2SO4 | 有氣泡產生 | NaOH和H2SO4發生了化學反應 |
B | 向某溶液中滴加BaCl2溶液 | 有白色沉淀 | 原溶液含有SO42﹣ |
C | 向集滿CO2的軟塑料瓶中加入約 | 塑料瓶變癟, 溶液變紅 | CO2能與石蕊反應 |
D | 將質量相同的Mg、Zn分別投入到足量的稀HCl中 | 鎂條表面產生氣體更多、更快 | 金屬活動性:Mg>Zn |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為了探究分子是否運動,張亮設計了如圖1所示的實驗。
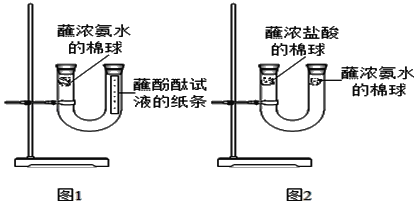
(1)一段時間后,可見圖1中酚酞的液點由下往上依次變紅色,他得出了結論_____,但陳紅覺得張亮的實驗還不足以證明,她又補充了實驗,你覺得沒有必要的是_____(填序號)。
A 用酒精燈對U型管加熱
B 向少量濃氨水中滴加酚酞試液
C 取少量濃氨水放在空氣中看是否變色
D 在U型管外放一條相同的酚酞試液紙條
酚酞變色,而棉球沒有變色,說明濃氨水和酚酞兩種物質中_____具有揮發性。
(2)陳紅還想探究分子運動速率與哪些因素有關,她說:“我們已經知道:溫度越高,分子運動速率越_____,但“可能還與相對分子質量的大小有關”畫線部分的話語屬于陳紅在_____(填序號)。
A 設計實驗 B 提出假設 C 描述現象 D 分析結論
她查找了資料:濃鹽酸易揮發出HCl,濃氨水易揮發出NH3.HCl和NH3會反應產生白煙(白煙成分為NH4Cl),然后按圖2所示固定裝置,在U型管管口分別塞上脫脂棉,各滴加一定量濃鹽酸、濃氨水,用橡皮塞塞緊,幾分鐘后,觀察到U型管_____(“左側”、“中間”或“右側”)出現較多白煙,說明相對分子質量越小,分子運動速率越快。
(3)生成的白煙NH4Cl可以作為一種氮肥,質量為多少千克的NH4NO3中氮元素質量與10.7千克的NH4Cl中氮元素質量是相等的?_____(請寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為粗略測定某石灰石中碳酸鈣的含量進行如下實驗。(裝置氣密性良好,雜質不參與反應)
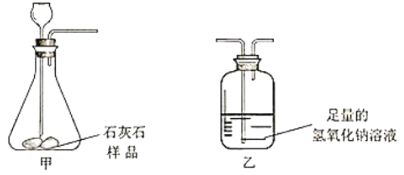
步驟I:稱量裝置甲和盛放的石灰石樣品的總質量;裝置乙和盛放的氫氧化鈉溶液的總質量。步驟II:連接裝置甲和乙,鹽酸由長頸漏斗加入到錐形瓶中至氣泡不再產生為止。
步驟III:二氧化碳被完全吸收后,測得裝置甲及其盛放的藥品增重了37.8克;裝置乙及其盛放的藥品增重了2.2克。
(1)鹽酸中的溶質是______(填寫名稱)。
(2)二氧化碳與氫氧化鈉溶液反應的化學方程式是______。裝置乙吸收的二氧化碳為______摩爾。
(3)該石灰石樣品中碳酸鈣物質的量_____。(根據化學方程式列式計算)
(4)實驗中所加的鹽酸溶質質量分數可能為______(選填編號)。
a 5% b 7% c 10%
(5)如所用的鹽酸溶質質量分數過大,對碳酸鈣含量測定結果的影響是______(選填“偏大”“偏小”或“無”),理由是______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室制取某些氣體所需的裝置如圖所示,請回答下列問題:
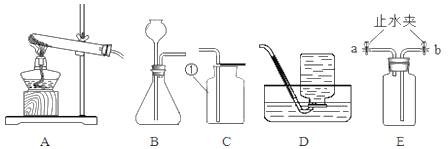
(1)實驗儀器①的名稱是______
(2)實驗室制取二氧化碳氣體應選擇的發生裝置是______(填選項字母)。該同學想要用E裝置除去CO2中的氯化氫雜質,則該裝置中盛放的物質是______;寫出該裝置中有關反應的化學方程式:______。
(3)選擇收集氣體方法時,必須考慮的氣體性質有______(填序號)。
①顏色②密度③溶解性④可燃性
(4)若用裝置E排水收集氧氣,瓶內先裝滿水,氣體從______(填“a”或“b”)導管通入瓶內。
(5)若選A裝置作為用高錳酸鉀制取氧氣的發生裝置,還須補充的一種用品是______,反應的化學方程式為______
查看答案和解析>>
科目:初中化學 來源: 題型:
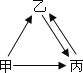
【題目】甲、乙、丙三種物質均含地殼中含量最多的元素.甲、乙是組成元素完全相同 的化合物,丙是單質;乙通常為液體,在一定條件下可分解生成丙;它們之間有如右圖所示的轉化關系(部分物質和反應條件已經略去).則:
甲的化學式為 ;乙分解生成丙的化學方程式為 .
從微觀的角度解釋甲、乙性質有差異的原因是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學興趣小組在老師的指導下進行課外實驗,利用下列裝置來探究磷單質在空氣中燃燒后氧氣濃度的變化情況。
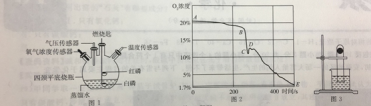
(提出問題)足量紅磷在密閉的四頸平底燒瓶內充分燃燒,熄滅后,容器中是否有氧氣剩余?
(猜想假設)猜想①:有氧氣剩余;
猜想②:無氧氣剩余。
(實驗驗證)該小組同學按如圖1組裝好實驗裝置,用高能激光筆分別照射燃燒匙上的紅磷和白磷,紅磷燃燒直至熄滅,白磷無明顯變化;待裝置完全冷卻后,將裝有白磷的燃燒匙提出水面,再次用高能激光筆照射,白磷被點燃。
(1)激光筆的作用是________________________。
(2)紅磷的燃燒產物與瓶底熱水反應生成磷酸(H3PO4)的化學方程式_________________ 。
(3)實驗過程中燃燒匙內的白磷第一次未燃著的原因是_________________ 。
(實驗結論)根據上述實驗現象,得出如下結論
(4)結論1:猜想_______正確
結論2:課本上“燃燒紅磷測定空氣中氧氣含量”的方法是_____(選填“嚴謹”或“不嚴謹”)的,其理由是_________________ 。
(注意:若答對第(5)(6)小題獎勵4分,化學試卷總分不超過60分。)
(拓展延伸)如圖2是該小組同學從開始實驗到最后裝置冷卻后的整個實驗過程中,用氧氣傳感器測量容器內氧氣濃度變化的曲線圖
(5)在圖中_____ (選填“A”“B”“C”“D”或“E")點時紅磷燃燒熄滅。請你解釋曲線AB段、DE段氧氣濃度變化的主要原因
①________________________。
②________________________。
(6)小組同學通過查閱資料得知,能夠較精確地驗證空氣中氧氣體積分數的藥品是鐵絲絨,利用鐵與氧氣、水等的緩慢氧化,可以將空氣中的氧氣濃度消耗至0.2%。將足量細鐵絲絨固定于試管底部,并倒扣在裝有水的燒杯中(如圖3),一段時間后你將看到的現象是________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】常溫下,向一定量的碳酸鈉溶液中不斷加入氫氧化鋇粉末,溶液質量的變化情況如圖所示。對該圖的分析有如下幾種說法,正確的是
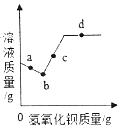
A. 向a點溶液中滴加無色酚酞溶液,溶液變紅,可證明有氫氧化鈉生成
B. 取少量b點溶液,滴入過量稀鹽酸,有氣泡產生
C. c點溶液中的溶質只有氫氧化鈉
D. 該溫度下,向d點溶液中加入氫氧化鋇粉末,溶質質量不變
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學興趣小組做了如圖所示實驗,當向乙燒杯中依次加入MnO2和H2O2溶液時,發現有大量氣泡產生,并產生大量白霧,蠟燭燃燒更旺,但過一會兒逐漸熄滅。而甲燒杯中蠟燭一直持續燃燒。
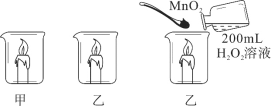
(知識回憶)寫出過氧化氫分解產生氧氣的化學方程式:_____。
(問題1)導致乙燒杯中蠟燭熄滅的原因是什么?
(作出猜想)猜想一:燃燒產生的CO2使蠟燭熄滅;
猜想二:白霧是水霧導致蠟燭熄滅;
小組同學經過討論,排除了猜想一,其理由是_____。
(實驗1)向一只裝有燃者蠟燭的燒杯中加入100℃水,另一只依次加入MnO2和H2O2溶液,若觀察到_____的現象,則猜想二正確。
(查閱資料)水霧產生與H2O2溶液的溶質質量分數大小有關,并且H2O2溶液的溶質質量分數越大,產生的水霧越多。
(問題2)為什么H2O2溶液的溶質質量分數越大水霧越多呢?
(實驗2)分別向三只燒杯依次加入MnO2和溶質質量分數的不同H2O2溶液測定溫度變化。
H2O溶液 | 5% | 10% | 30% |
溫度變化曲線 |
|
|
|
(解釋與結論)
(1)該對比實驗過程中不需要控制的條件是_____。
A H2O2溶液的初始溫度相同 B 反應開始的時間相同 C 二氧化錳的質量相同
(2)根據實驗2,可得出的一個結論是_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com