
【題目】化學興趣小組的同學對“影響金屬與鹽酸反應的劇烈程度的因素”進行了探究。
【提出問題】金屬與鹽酸反應劇烈程度受哪些因素的影響?
【做出猜想】a.可能與金屬本身的性質有關;b.可能與鹽酸的濃度有關。
【設計探究】實驗所用金屬均已用砂紙打磨。
(1)【實驗Ⅰ】為探究猜想a,小組同學分別在兩支試管中放入相同質量的鋅片和鐵片,然后分別加入等質量、等濃度的稀鹽酸,觀察到放鋅片的試管中立即產生大量氣泡,放鐵片的試管中只產生少量氣泡。寫出鋅與鹽酸發生反應的化學方程式:。從實驗現象可判斷金屬活動性:Zn(選填“<”“=”或“>”)Fe。
(2)【得出結論】金屬與鹽酸發生反應的劇烈程度與金屬本身性質有關,金屬的活動性與反應的劇烈程度的關系是。
(3)【實驗Ⅱ】為探究猜想b,小組同學設計如圖的裝置進行實驗,其中注射器的作用是。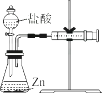
(4)所用藥品、實驗數據如表:
實 | 選用 | 鹽酸質 | ||||||
產生氫氣的體積/mL | ||||||||
第 | 第 | 第 | 第 | 第 | 前5分鐘 | |||
Ⅰ | 鋅片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 鋅片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【得出結論】金屬與鹽酸發生反應的劇烈程度與鹽酸的濃度有關,其關系是。
(5)【反思評價】根據表中實驗Ⅱ數據分析,請解釋鋅與鹽酸反應最后變慢的原因: 。
【答案】
(1)Zn+2HCl=ZnCl2+H2↑,>
(2)金屬活動性越強,反應越劇烈
(3)通過注射器往右移動的體積測得生成氫氣的體積
(4)其他條件相同時,鹽酸濃度越大,反應越劇烈
(5)鹽酸濃度變小,反應速率減慢
【解析】(1)【設計探究】由題意知:反應物、生成物,根據質量守恒定律,正確書寫化學方程式,鋅與鹽酸反應的化學方程式為:Zn+2HCl=ZnCl2+H2↑;放鋅片的試管中立即產生大量氣泡,放鐵片的試管中只產生少量氣泡,因此金屬活動性強弱為:Zn>Fe;
(2)得出結論:金屬與鹽酸反應的劇烈程度與金屬本身性質有關(金屬活動性越強,反應越劇烈);
(3)實驗(2)注射器的作用是通過注射器往右移動的體積判斷生成氫氣的體積;
(4)得出結論:根據表格信息可知,其他條件相同時,鹽酸濃度越大,反應越劇烈;
(5)【反思評價】鋅與鹽酸反應產生氣體的速度先加快后變慢,因為鋅與鹽酸是放熱反應,所以開始時溫度升高,產生氣體速度加快,隨著反應的進程,鹽酸不斷被消耗,濃度降低,產生氣體速度變慢.
故答案為:(1)Zn+2HCl=ZnCl2+H2↑;>;(2)金屬活動性越強,反應越劇烈;(3)通過注射器往右移動的體積判斷生成氫氣的體積;(4)
其他條件相同時,鹽酸濃度越大,反應越劇烈;(5)鹽酸濃度變小,反應速率減慢.
(1)鋅和稀鹽酸反應生成氯化鋅和氫氣;根據現象得出結論;
(2)根據金屬的活動性順序,分析金屬的活動性與反應的劇烈程度的關系;
(3)注射器的作用是量取生成氣體的體積;
(4)根據表中信息結合濃度對反應的影響分析解答;
(5)表中信反應的劇烈程度與酸的濃度有關,結合反應的過程進行分析解答即可.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
【題目】下列實驗現象描述正確的是( )
A.用石蕊溶液染成的干燥的紫色紙花放入二氧化碳中,紙花變紅
B.一氧化碳還原氧化鐵的反應中,黑色粉末變成了紅色
C.硫在空氣中燃燒發出微弱的淡藍色火焰,生成有刺激性氣味的氣體
D.氧化鐵與稀鹽酸反應,溶液由無色變成淺綠色
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】隨著人們生活水平的不斷提高,汽車已走進千家萬戶。制造汽車要用到含銅、鐵、鋁等成分的多種金屬材料。
(1)在汽車電路中,經常用銅做導線,這是利用了銅的性;
(2)工業上用CO還原赤鐵礦冶煉金屬鐵的化學方程式為;
(3)汽車使用的金屬材料多為合金,是因為合金與純金屬相比,具有(填一條)等優良性能。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列各組離子在同一溶液中一定能大量共存的是( )
A.H+、K+、OH﹣、Cl﹣
B.H+、Na+、Cl﹣、SO42﹣
C.Ba2+、Cu2+、CO32-、NO3-
D.CO32-、OH-、Na+、Ca2+
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列實驗現象描述正確的是
A.硫在空氣中燃燒發出淡藍色火焰,生成一種無色無味的氣體
B.電解水實驗中,與電源正極相連的容器內產生的氣體體積大
C.鐵絲在空氣中劇烈燃燒,火星四射
D.向硫酸銅溶液中加入氫氧化鈉溶液,生成藍色沉淀
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com